
의료제품 중 사전상담을 통해 보다 빠르게 허가를 받을 수 있는 품목은 무엇일까.
식약처 식품의약품안전평가원 제품화지원팀은 최근 '의료제품의 사전상담 업무 안내서' 개정을 통해 이같은 내용을 소개했다. 이번 개정은 지난달 의료제품의 사전상담 운영 규정 예규 개정 반영 등 현행화를 진행했다.
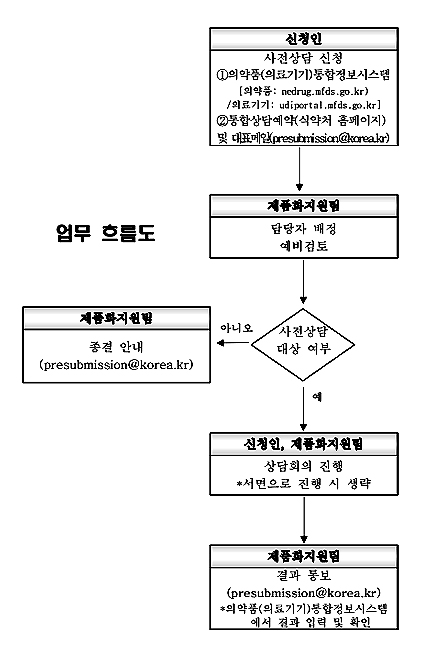
식약처는 제품화지원팀 주관 사전상담을 진행하고 있다.
먼저 사전상담 대상은 생명을 위협하거나 중대한 질환의 치료를 목적으로 하는 의약품으로 기존 치료법이 없거나 기존 치료법보다 유효성 등에서 의미 있는 개선을 목적으로 하는 경우, 희귀약이나 개발단계희귀약, 생물테러감염병 또는 감염병의 대유행 등 공중보건의 심각한 위해를 끼칠 우려가 있는 감염병의 예방이나 치료 목적 의약품, 이들 이외의 신약, 희소의료기기, 혁신의료기기, 혁신기술 적용 융복합 의료제품이다.
여기서 의약품의 경우 생물학적제제, 유전자재조합의약품, 한약(생약)제제를 포함한다.
다만 첨단바이오약은 세포유전자치료제과가, 희소체외진단의료기기나 체외진단의료기기는 체외진단기기과, 혁신의료기기 중 디지털헬스기기는 디지털헬스규제지원과에서 담당한다.
범위는 임상시험계획 승인 신청전 단계 및 품목허가 신청전 단계에서 기준및시험방법 등 품질, 의료기기 등 기술문서, 비임상시험, 임상시험 등과 관련된 사항이 사전상담대상이다.
반면 제조 및 품질관리기군에 대한 사항이나 동일 목적의 이전 사전상담이 개최된 이후 유의미한 새로운 정보가 추가되지 않은 경우, 사전 검토 대상은 사전상담대상에서 제외된다.
사전검토의 경우 법적 효력이 있으며 완결성이 높은 자료를 허가 신청 전에 미리 검토받고자 할때 진행되며 구체적인 자료를 제출해 적합여부 검토, 현 개발단계에서 법적 효력있는 규제기관의 방향과 의견이 제공된다.
사전상담은 법적 효력이 없으며 다음 단계 진입을 위해 이전 자료를 근거로 방향과 계획에 대해 검토 받고자 할 때 진행되며 여러가지 가능성과 방법을 검토해 구체적이고 다양한 의견 제시가 가능하다.
제출자료는 사전상담 대상 설명자료, 해당 제품에 대한 정보로 의약품의 경우 구성 성분, 작용 기전, 제조방법, 예상 효능효과 등을, 의료기기는 의료기기 허가신고심사 등에 관한 규정, 제26조 및 제29조 중 해당하는 자료, 개발 정보로서 품질, 의료기기는 기술문서, 비임상시험, 임상시험요약자료 등이다. 또 개발제품에 대한 국내외 현황 및 유사품목과의 비교 자료, 질의사항 등을 신청서와 함께 제출한다.



