리제네론, 위탁사 캐털란트 제조결함 해결 8월중순 재제출 진행
투약기간을 늘린 고용량(8mg) 황반변성 치료제 아일리아에 대한 FDA 승인이 빠르면 3분기내 완료될 것으로 전망됐다.
리제네론은 3일 2분기 및 상반기 실적보고를 통해 지난 6월 27일 FDA로 부터 완결된 응답서신을 접수받아 승인거부된 고용량 아일리아 승인신청 관련 재승인신청과 FDA의 조기검토를 통해 3분기내 승인을 받을 수 있을 것으로 기대했다.
리제네론은 CRL은 위탁제조사인 캐털란트(Catalent)의 바이알 충전관련 문제로 CRL이 접수됐으며 효능과 안전성 프로필, 라벨링, 약물제조 관련 문제는 없었다며 위탁사의 충진문제 해결을 통해 8월 중순경 재신청을 진행할 수 있것이라고 밝혔다.
이어 FDA의 우선검토 진행의지를 확인한 만큼 올해 3분기에 승인여부에 대한 조치가 취해질 것으로 기대했다.
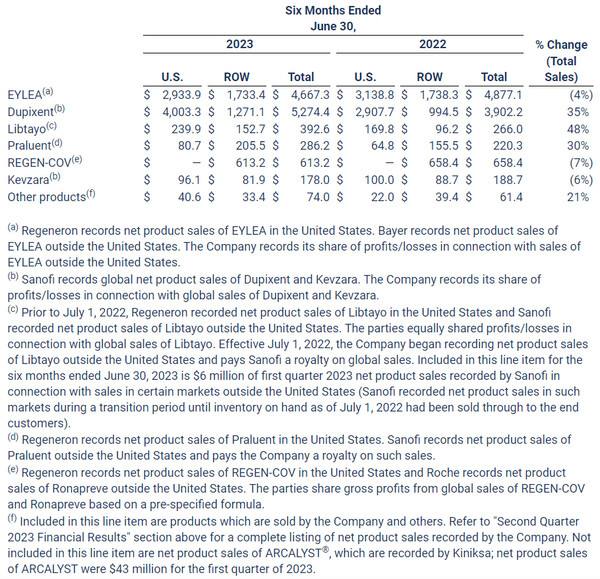
한편 리제네론은 2분기 31억 5800만 달러의 매출을 올려 전년동기 28억 5700만달러 대비 11% 성장했다.
이는 아일리아의 미국내 직접판매 매출의 감소와 바이엘의 협업판매 매출의 부진에도 사노피의 듀피젠트 매출증가가 매출신장에 도움을 준데 영향이 크다.
저작권자 © 뉴스더보이스헬스케어 무단전재 및 재배포 금지



