오츠카·룬드벡, 자문위 9:1 승인권고 기반...국내생산 수출품목

렉설티가 최초의 알츠하이머병 초조증상 치료제로 FDA 승인을 받았다.
오츠카와 룬드벡은 11일 렉설티(브렉스피프라졸)가 알츠하이머병으로 인한 치매환자의 초조증상 치료를 적응증으로 FDA로 부터 추가 승인을 받았다고 밝혔다. 앞서 FDA 자문위는 9:1의 의견으로 이점이 위험을 능가한다고 투표, 승인을 권고하는 의견을 제시했다.
승인은 투약 12주차에 1차 평가변수인 초초함 척도(CMAI/Cohen Mansfield Agitation Inventory)를 위약대비 5.32점(31%) 더 개선한 31-14-213(NCT03548584) 3상 임상결과를 기반으로 한다.
이번 승인으로 렉설티는 FDA의 승인을 받은 최초이자 유일한 알츠하이머 초조증치료제가 됐다. 렉설티의 기존 적응증은 주요우울장애 치료의 부가요법과 13세 이상 조현병 등으로 2015년 FDA 승인을 받았다.
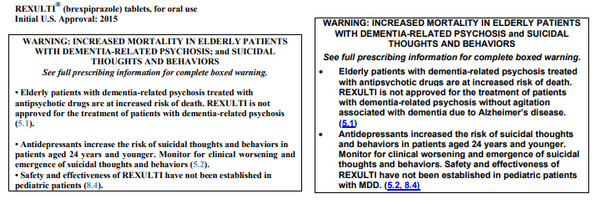
반전에 가까운 렉설티의 적응증 승인에 따라 기존 블랙박스 경고 문구도 변경됐다.
"기존 치매성 정신질환을 겪는 노인환자의 사망위험 증가하며 렉설티는 이에대해 승인되지 않았다"에서 10일자 변경 블랙박스 문구는 "알츠하이머병을 원인으로 하는 치매를 제외한 치매성 정신질환자에는 승인되지 않았다"로 바뀌었다.
국내에는 2018년 수출용으로만 허가를 받았다. 즉 국내 생산되는 몇 안되는 글로벌 신약이다.
저작권자 © 뉴스더보이스헬스케어 무단전재 및 재배포 금지



