시험약의 비교대상이 되는 대조약을 신청하기 전에 반드시 확인하고 고려해야할 사항은 과연 무엇일까?
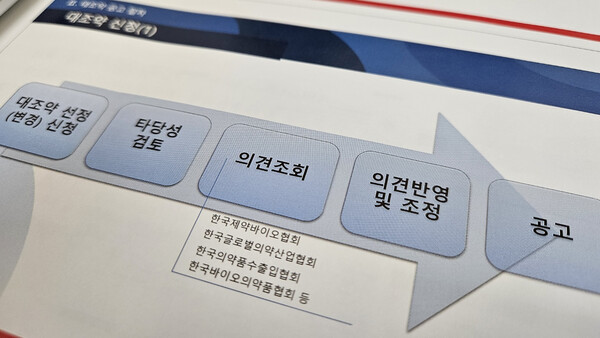
식약처는 20일 '2024년 의약품 허가심사 설명회'에서 대조약 공고 절차에 대해 안내했다.
먼저 대조약 신청 전 확인사항의 경우 '의약품 등의 안전에 관한 규칙' 제조판매-수입 품목의 허가신청에 따른 품목인지, 기존에 공고 대조약이 존재하는지 확인이 필요하며 신약은 신약 지정 목록 또는 신약임을 알 수 있는 허가즌, 원개발사 품목은 R&D 포커스, 파마프로젝트 등 공신력 있는 입증자료 등을 살펴야 한다.
또 자료제출의약품은 '의약품의 품목허가-신고-심사 규정' 안전성-유효성심사 자료제출의약품에 해당하는 자료를 제출해 허가받은 품목임을 알 수 있는 자료인 허가증, 심사 또는 검토결과 정보공개 보고서 등과 생동 인정푸목 목록 등과 성방성제제는 제제학적 차이를 입증할 수 있는 자료 등을 우선 확인해야 한다.
그럼 선정에 있어 추가적으로 고려되는 사항은 무엇일까.
추가 선정이 가능한 경우는 기존 대조약이 원개발사 품목이 아닌 경우 원개발사 품목 국내 허가시 대조약으로 추가 선정이 가능하다. 동등성 시험 시 우선 사용된다.
아울러 제형 또는 함량 등의 특수성이 인정되는 경우 별도 선정된다. 서방성제제, 1일 최대 허용량 범위내에서 생동시험이 불가능한 경우, BCS 근거 생동면제 인정가능 성분 등이다. 여기에 동일한 일자에 허가된 신약은 추가 선정이 가능하다.
반면 선정에 제한이 되는 경우도 있다.
공동으로 생동 또는 임상시험을 진행해 동일한 날짜에 품목허가(신고)된 경우 핵심 임상시험 주관 업체의 품목을 선정하며, 생동 대조약은 투여경로가 동일한 제형 및 함량별로 선정하지 아니하고 화학적 기본골격이 동일한 품목은 추가 선정하지 않는다. 예를 들어 이성체, 염류 및 체내에서 기허가 품목과 동일한 활성모핵을 전환되는 에스테르화합물 등이 이에 해당된다.
해외 대조약 사용요건은 기존 대조약이 미생산(미수입) 등으로 국내 유통되지 않은 경우 해당 업체로부터 대조약이 국내 판매되지 아니함이 확인되고 외국에서 구입한 의약품이 국내 대조약과 제조소,표시기재 등을 통해 동일성을 입증한 경우 동등성 시험에 사용이 가능하다.
한편 대조약의 취소는 품목취소 도는 취하된 경우나 대조약의 제조수입 실적이 제품의 사용기간 이상 중단됐음을 확인할 수 있고 대조약 업체에 생산(수입)계획 요청시 구체적인 일정이 없거나 미제출시 이뤄진다.



