
정부가 혁신형 제약기업 인증요건과 평가방식을 개선하기로 했다. 의약품 연구개발비 비율 요건을 상향 조정하고, 유형을 일반·벤처·외국계로 나눠 특성별 평가항목을 마련하는 게 골자다.
이 같은 사실은 보건복지부가 최근 공개한 '제3차 제약·바이오산업 육성·지원 시행계획(2023)' 자료를 통해 확인됐다.
29일 관련 자료를 보면, 연내 혁신형 제약기업 인증제도 리뉴얼에 나선다.
인증 유형 구분=복지부는 신약 연구개발 주체가 다양한 유형으로 변화됨에 혁신형 제약기업 유형을 구분하기로 했다.
현재는 기업 규모·유형과 관계없이 단일 심사체계로 돼 있는 데 이를 일반·벤처형으로 구분해 기업별 특성을 반영한 심사체계로 변경하기로 한 것이다. 벤처사는 벤처기업육성법에 따른 벤처기업(창투사 등이 5천만원 이상 투자, 기업 자본금 중 투자금 비율 10%) 중 신약 연구개발을 전문으로 하는 기업을 의미한다.
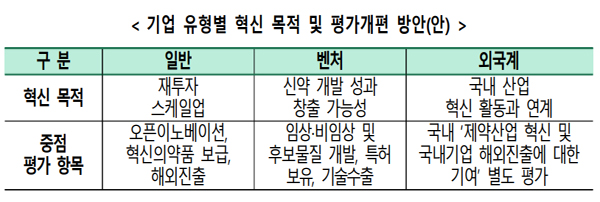
유형별 맞춤형 평가를 위해 평가항목별 배점도 차별화한다. 또 연구개발 투자 촉진을 위해 의약품 연구개발비 비율 요건을 2~3%p 상향하기로 했다. 현재는 매출액 1천억원 미만 기업 7%, 1천억원 이상 기업 5%, 미국·EU GMP 획득기업 3% 이상으로 돼 있다.
이와 함께 외국계 제약사의 국내 협업을 촉진할 수 있는 별도의 인증요건 신설도 검토한다. 또 기업 유형별 차별화된 평가와 함께 배점조정, 정량평가 확대, 유사중복지표 간소화 등 평가방식도 개선한다. 정량평가 확대와 관련해서는 연구개발비, 연구개발 인력(또는 박사급 연구개발 인력 비율) 등을 예시했다.
맞춤형 지원 확대=혁신형 제약기업 중 벤처형을 대상으로 정책펀드 우선 지원방안과 R&D 가점 부여방안을 검토한다. 기업간 협업(오픈이노베이션)으로 엑셀러레이팅, 공동연구, 공동투자 등에 대한 별도 R&D 지원방안도 모색한다.
의약품 품질 제고 및 제조생산 공정 최적화를 위한 QbD 컨설팅 지원과 산·학·연·병 공동연구 및 기술협력 활성화, 글로벌 기술수출, M&A 등 연계활동 지원 방안도 검토대상에 포함시켰다. 이밖에 정부 R&D 우선 참여 혜택도 전부처 사업으로 확대 추진한다.
재인증=지속적인 연구개발 투자 확대 및 혁신 성과 창출을 위해 재인증 기준 강화방안도 마련하기로 했다.



