2세 이상 유아 아토피피부염 환자를 위한 국소도포제형의 치료옵션이 대거 확대될 전망이다.
듀피젠트 이외 추가치료 옵션의 확대가 제한적인 12세 이하 어린이 아토피피부염 환자를 위한 3품목의 국소도포제 임상개발이 순조롭게 진행되고 있다. 품목은 졸리브, 비타마, 옵제루라 등이다.
아쿠티스는 19일 건선을 적응증으로 승인받은 졸리브(Zoryve, 로플루밀라스트)의 2~5세 유아 아토피피부염 환자 대상 2건의 병행 3상임상 결과를 발표했다. 이를 기반으로 규제승인을 진행한다는 계획이다.
INTEGUMENT-1와 2 등 2건의 3상에서 4주차에 1일 1회 졸리브 투약군의 EASI-75 달성비율은 39.4%로 위약군 20.6%, 연구자평가인 IGA 0/1 달성비율도 25.4% 대 10.7%였다.
가려운증 척도(WI-NRS)에서도 4점이상 감소비율은 35.3%대 18.0% 등으로 모든 평가변수를 충족했다. 또 임상에 참가한 어린이 93.8%가 임상을 종료했으며 이중 93.4%는 장기치료효과를 살피는 INTEGUMENT-OLE 연구에 참여키로 했다.
아쿠티스는 지난 9월 12일 아토피피부염 환자6세 이상 어린이와 성인에 대한 추가적응증 승인신청서를 제출했으며 이번 2세 이상 임상데이터를 기반으로 추가 승인을 추진한다는 계획이다.
더바반트, 비타마 2세 이상 3상 완료...승인신청 전
건선치료제로 FDA 승인을 받은 비타마(Vitama) 역시 2세 이상 어린이와 성인환자 대상 2건의 3상을 완료, 규제승인을 준비중이다.
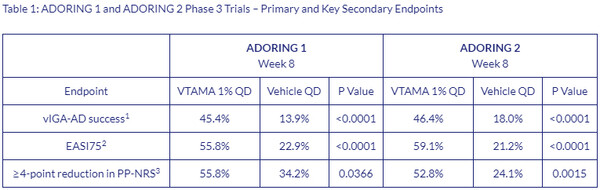
ADORING 1과 2 등 병렬진행 3상에서 8주차에 EASI75달성비율은 각각 55.8%, 59.1%로 위약대조군 22.9%, 21.2% 대비 개선을 제시했다.
인사이트 옵제루라 2~12세 관련 3상 임상 완료
TRuE-AD3 3상의 완료소식을 7월 발표한 인사이트는 아직 세부적인 임상데이터를 발표하지 않았다. 임상은 미국과 캐나다 북미지역에서만 진행됐으며 329명을 대상으로 진행됐다. 1차 평가변수는 연구자 평가기준(IGA-TS) 2점이상 개선된 0,1(거의 깨끗함 이상) 달성 비율을 위약대조 평가했다.
가장 앞서 아토피피부염 치료를 위한 국소도포제로 승인됐으나 소아환자 대상 임상개발속도가 더디다.
현재 2세 이상의 환자가 활용할 수 있는 비스테로이드 국소도포제는 FDA 승인기준 프로토픽, 엘리델, 유크리사 등 3품목이 있다.
이중 가장 최근인 2016년 승인된 유크리사는 2020년 생후 3개월이상으로 적응증 영역을 확대한 바 있다. 다만 유크리사는 국내승인을 받지 않았다.
3가지 품목이 모두 승인된다면 유아 아토피피부염 환자가 활용할 수 있는 치료옵션이 두배 증가하게 되며 아릴 탄화수소 수용체 작용제(비타비)와 JAK억제제(옵제루라)라는 새로운 기전이 추가되게 된다.



