키트루다+렌비마 병용, 신세포암·자궁내막암 적응증 허가

한국MSD는 ‘키트루다(성분 펨브롤리주맙)’가 12월 22일 식품의약품안전처로부터 에자이의 경구용 다중 키나아제 억제제 ‘렌비마(성분 렌바티닙)’와의 병용요법으로 진행성 신세포암 1차 치료제 및 3상 임상시험 기반 진행성 자궁내막암 치료제로 적응증을 허가받았다고 11일 밝혔다.
키트루다는 렌비마와 병용요법으로 신세포암 1차 치료제로 새롭게 허가 됐다. 신세포암 치료에서 키트루다-렌비마 병용요법은 23.9개월의 무진행 생존기간 중앙값을 기록했다.
이번 허가는 3상 임상인 CLEAR 연구(KEYNOTE-581/Study 307)를 기반으로 이루어졌다. CLEAR 연구를 통해 키트루다-렌비마 병용요법은 기존 치료법인 수니티닙 대비 통계적으로 유의미한 무진행 생존기간(Progression-Free Survival, PFS) 및 전체 생존기간(Overall Survival, OS) 개선효과를 입증했다.
연구에 따르면 키트루다-렌비마 병용요법은 수니티닙 대비 질병 진행 또는 사망 위험을 61%(HR=0.39 [95% CI, 0.32-0.49]; p<0.001) 감소시킨 것으로 나타났으며, 사망 위험은 34%(HR=0.66 [95% CI, 0.49-0.88]; p=0.005) 감소했다.
전체 생존기간은 중앙값에 도달하지 않고 지속되고 있다. 키트루다-렌비마 병용요법의 객관적 반응률(Objective Response Rate, ORR)은 71%, 수니티닙군은 36%를 기록했고 완전관해(Complete Response, CR)는 각각 16% vs. 4%, 부분관해(Partial Response, PR)는 각각 55%, 32%로 나타났다. 임상에서 가장 빈번하게 관찰된 이상 반응은 설사와 고혈압이었다.
또 2020년 5월 2상 임상(KEYNTOE-146/Study 111)을 기반으로 렌비마 병용요법으로 승인되었던 키트루다의 자궁내막암 적응증은 3상 임상인 ‘KEYNOTE-775/Study 309’ 기반으로 허가 받았다. KEYNOTE-775/Study 309는 이전의 전신요법 이후 질병 진행이 확인된 진행성 자궁내막암을 대상으로 50년 만에 성공한 3상 임상이라는 점에서 의미가 크다.
키트루다의 국내 허가사항은 기존과 동일하게 이전의 전신요법 이후 진행이 확인되고 수술 및 방사선 치료가 부적합한, 고빈도-현미부수체 불안정성(microsatellite instability high, 이하 MSI-H) 또는 불일치 복구 결함(mismatch repair deficient, 이하 dMMR)이 없는 진행성 자궁내막암 치료로서 렌비마와 병용요법이 사용된다.
연구 결과, 키트루다-렌비마 병용요법은 화학요법(독소루비신 또는 파클리탁셀) 대비 사망 위험을 32%(HR=0.68 [95% CI, 0.56-0.84]; p=0.0001) 감소시키고, 질병 진행 또는 사망 위험은 40%(HR=0.60 [95% CI, 0.50-0.72]; p<0.0001) 감소시켜 전체 생존기간과 무진행 생존기간 모두에서 통계적으로 유의한 개선을 확인했다.
키트루다-렌비마 병용요법의 전체 생존기간 중앙값은 17.4개월(95% CI, 14.2-19.9), 화학요법은 12개월(95% CI, 10.8-13.3), 무진행 생존기간 중앙값은 각각 6.6개월(95% CI, 5.6-7.4), 3.8개월(95% CI, 3.6-5.0)로 나타났다. 데이터는 MSI-H 또는 dMMR이 없는 697명의 환자를 대상으로 분석됐다.1 중대한 약물이상반응(≥3%)은 키트루다와 렌비마를 병용 투여한 환자 50%에서 발생했으며, 고혈압(4.4%), 요로감염(3.2%) 순으로 나타났다.
메드트로닉, 인슐린 펌프 ‘미니메드 770G 시스템’ 출시
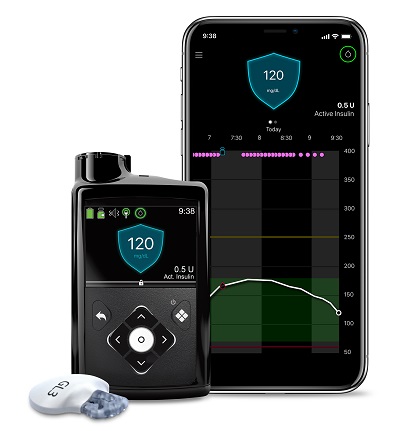
메드트로닉코리아는 연속혈당측정기(CGM) 기능 연동형 인슐린 펌프인 ‘미니메드 770G 시스템(MiniMed 770G)’을 국내에 출시했다고 11일 밝혔다.
인슐린 펌프는 췌장에서 인슐린을 생성하지 못하는 자가면역 질환인 제1형 당뇨병이나 인슐린 의존형 당뇨병 등으로 혈당 관리에 어려움을 겪는 환자들의 인슐린 주입과 관리를 돕는 의료기기다.
이번에 출시된 ‘미니메드 770G 시스템’은 국내에 허가된 센서 연동형 인슐린 펌프인 ‘미니메드 640G 시스템’의 후속 제품으로 환자에 따른 맞춤형 치료가 가능하도록 편의 기능을 대폭 강화했다.
먼저 환자의 혈당을 5분마다 모니터링하고, 그에 맞춰 기저 인슐린 주입량을 자동으로 조절하는 스마트가드 (SmartGuard) ‘자동 모드’ 기능이 추가됐다. 목표 혈당값을 유지하기 위해 센서 포도당 값이 올라가면 인슐린 주입 용량을 증가시키고, 센서 포도당 값이 내려가면 인슐린 주입 용량을 줄여 환자가 저혈당 및 고혈당 위험에 노출되지 않도록 돕는다. 목표한 범위 내에 혈당을 유지시킬 수 있도록 도울 뿐 아니라, 일정 조건이 충족되면 24시간 자동 혈당 관리가 가능해 환자 편의성이 증대됐다.
또한 환자와 보호자를 위한 스마트폰 앱을 통해 인슐린 펌프의 데이터를 쉽고 편리하게 확인할 수 있게 됐다. 인슐린 펌프 사용자는 블루투스로 전송된 데이터를 ‘미니메드 모바일 앱’을 통해 스마트폰 앱에서 바로 확인 가능하다. 보호자 역시 ‘케어링크 커넥트 앱’을 통해 실시간으로 펌프의 데이터를 스마트폰에서 확인하고, 알람도 받을 수 있어 스스로 관리가 어려운 소아 환자나 고령의 환자와 같은 경우 보호자가 혈당 관리 현황을 손쉽게 확인할 수 있다.



