지난 12일부터 개정 시행된 의약품동등성시험기준은 어떤 것들이 있을까.
식약처는 이에 지난 11일 규정개정에 따른 의약품동등성시험(이하 의동시험) 시 유의사항에 대해 공유하고 업계의 이해를 도왔다.
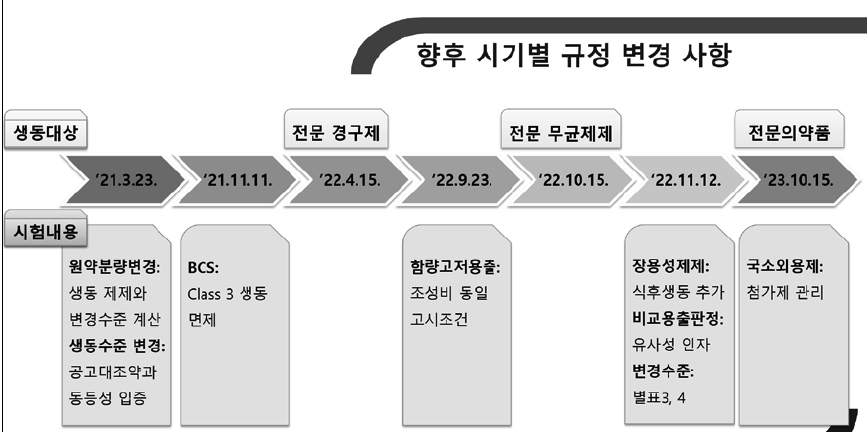
먼저 지난 12일부터 시행된 의동시험 기준 개정에 대해 간략하게 안내했다.
의동시험 적용범위는 지난 4월15일부터 경구용제제, 10월15일부터느 무균제제가, 내년 10월15일부터는 그외 제제가 적용대상이 된다.
이번에 시행딘 의동시험기준 개정 주요내용은 장용성제제의 식후 생동이 추가됐다.
생물학적동등성시험방법이 기존 식후 시험 추가 실시대상은 서방성제제만 포함됐으나 앞으로는 장용성제제도 이에 들어간다.
또 용출양상의 동등성 판정기준 및 유사성 인자, 판정기준이 개정됐다. 이는 국제조화를 위한 것이다.
기존 평균용출율 차이 또는 유사성 인자 둘 중 선택이었으나 앞으로는 유사성 인자로만 동등성을 판정하도록 개정됐다. 비교시점의 변이계수 적용 및 비교시점 기준을 강화한 것이다.
또 장용성 및 서방성제제의 경우 유사성 인자기준(50 이상) 및 모든 비교시점에서 평균용출률 차이(15% 이내)를 적용하게 된다.
여기서 변이계수는 대조약과 시험약 평균용출률의 첫번째 비교시점은 20%, 그 외 비교시점은 10% 이내이다.
생동 제외대상도 확대됐다.
기존 계열1 약물 생동성시험 면제서 계열1과 계열3 약물도 생동성시험이 면제된다.
여기에 경구용 고형제에서 경구용 고형제와 함께 현탁제도 새롭게 포함됐다. 이는 첨가제 기준 추가, 투과도 시험 등 ICH가이드라인 세부 내용이 반영됐다.
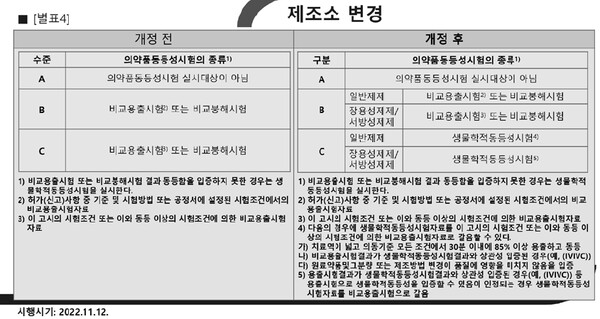
이밖에도 제조방법 변경, 제조소 변경도 이뤄졌다.
제조방법의 변경수준 및 제출자료의 범위가 기존 A~D로 나눴으나 앞으로는 크게 3가지로 구분된다. 품질에 영향이 없는 변경은 의동시험 실시대상이 아님, 경미한 변경은 비교용출시험 또는 비교붕해시험, 중요한 변경의 경우 크게 비교용철시험 또는 이화학적동등성시험 또는 비교붕해시험, 생물학적동등성시험으로 나뉜다.
제조소 변경의 경우 일반제제와 장용성제제-서방성제제로 세부적으로 나눴다. 특히 생물학적동등성시험이 추가됐다.



