전도유망해보이던 에자이와 바이오젠의 알츠하이머 치료제 후보약물 '레카네맙'이 치료효과를 제시한 3상 임상결과를 발표했다.
지난 9월 제한적인 정보만 제공됐던 Clarity AD(NCT03887455) 3상 초기임상결과는 뉴잉글랜드저널오브 메디신과 미국 샌프란시스코에서 열린 알츠하이머 임상회의를 통해 공개됐다. (https://www.nejm.org/doi/full/10.1056/NEJMoa2212948)
임상참가자는 1,795명, 이중 898명이 레카레맙을 897명은 위약을 투약받았다. 1차평가변수인 치매임상평가척도박스총점(CDR-SB/6개항목 총 18점)의 두그룹에서 약 3.2점이었다.
18개월차 CDR-SB의 기준점에서 변화는 레카네맙은 1.21점, 위약군에서 1.66점이었다. 즉 CDR-SB점수(높을수록 악화) 기준으로 0.45점 낮추는 결과를 보여줬다.
2차평가변수인 아밀로이드 부하감소는 -59.12, AD 인지평가척도(ADAS-cog14)는 -1.44 감소, 알츠하이머병 종합점수(ADCOMS) -0.05점 감소, 일상생활능령평가점수(ADCS-MCI-ADL) 2.0점 개선 등 모든 척도는 위약군 대비 레카네맙의 선호 경향성을 보였다.
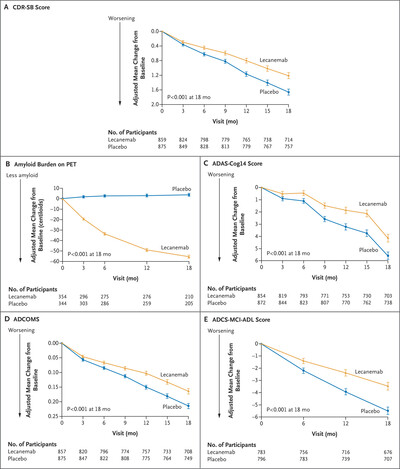
또한 투약기간이 늘어날 수록 알츠하이머 진행속도를 늦추는 효과를 제시했다. 1차 평가변수인 CDR-SB 점수의 개선은 크지 않으나 기존 약물에서 보여주지 못한 효과라는 점에 대해 이견은 적다. 위약 0.45점 차이가 유의미한 수준인가에 대해, 임상의들의 평가는 엇갈린다.
부작용은 투약관련 부작용을 제외하고 아밀로이드 관련 영상이상(ARIA), 관련 뇌부종(ARIA-E) 위험이 위약군보다 높았다.
사망은 레카네맙에서 0.7%(6명), 위약군에서 0.8%(7명)발생했으며 연구진은 레카네맙과 관련있거나 아밀로이드 관련 영상이상(ARIA)으로 간주되는 사망은 없었다고 설명했다.
다만 연구진의 견해와 달리 임상결과 발표 이틀전 사이언스지(27일자)에는 임상참가자의 뇌출혈 사망사건이 약물과 관련성을 배제할 수 없다는 주장이 제기된 바 있다. (https://www.science.org/content/article/second-death-linked-potential-antibody-treatment-alzheimer-s-disease)
연구진도 임상 초기결과에 대한 결론으로 아밀로이드 플라그의 감소시키고 18개월차에 위약대비 인지능력과 신체기능 저하속도를 약간 저하시켰으나 부작용과 관련이 있다고 레카네맙을 평가했다.
이어 레카네맙의 효과와 안전성을 확인하기위해 장기임상이 필요하다고 덧붙였다.



