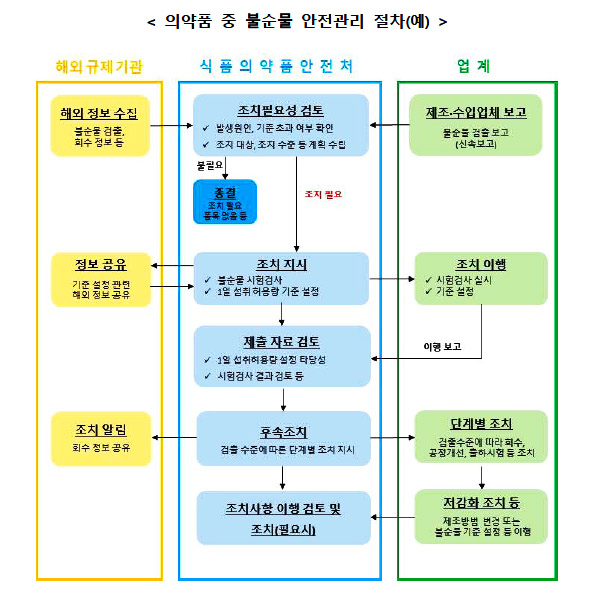
제약이 자사 의약품에서 불순물이 검출될때 그 검출 수준에 따라 조치해야할 사항은 무엇일까.
식약처는 최근 의약품 중 변이원성-발암성 불순물 안전관리 가이드라인을 통해 단계별 조치사항을 안내했다.
제약사는 불순물 검출량과 허용기준을 비교해 시중 유통중인 제품 중 기준을 초과한 제품(배치)에 대한 자진 회수 및 불순물 저감화 등 필요한 조치를 취해한 관련 사항을 식약처에 제출해야 한다.

단계별 조치사항을 보면 '수준1~수준4'로 나뉜다.
'수준1'의 기준 초과의 경우로 허용기준을 초과한 제품에 대해 즉시 판매중지 및 회수조치해야 한다. 제조공정 개선 등을 통해 저감화하거나 규격에 기준을 설정해 관리하고 제조공정을 개선해 허가변경 등을 허거나 허가변경 등을 완료 전까지 모든 제조번호별로 시험검사를 실시해 적합한 제품만 출하하면 된다.
'수준2'는 기준의 30% 초과에서 기준 이내의 경우로 기준을 초과한 제품은 없어 판매 중지 및 회수조치는 불필요하다. 다만 허용기준을 초과할 가능성은 상존하므로 제조공정 개선 등을 통해 저감화하거나 규격에 기준을 설정해 관리하고 '수준1'과 같은 방식으로 모든 제조번호별로 시험검사를 실시해 적합한 제품만 출하하면 된다.
'수준3'은 기준의 10% 초과에서 30%이하의 경우로 대표성 있는 제품을 선정해 주기적으로 시험검사를 하면 되며 다만 제조방법 변경, 규격 설정 등 허가변경이 수반되지 않는 경우에는 관련 사항을 제품표준서에 반영해 관리해야 한다.
'수준4'는 기준의 10% 이할 불순물 검출이 된 경우로 불검출된 것으로 간주해 시험 생략이 가능하다.
한편 2종 이상의 니트로사민 불순물 검출시 모든 니트로사민류의 총 발암 위해가 10⁻⁵이하로 관리될 수 있도록 자체적으로 관리하고 10⁻⁵ 초과시 허가변경이 필요하며 4종 이상의 니트로사민 불순물이 검출시 모든 니트로사민류의 발암 위해의 함이 10-5 이하로 간리될 수 있도록 자체적으로 기준 설정해 주기적인 관리를 해야 한다.