지난해부터 세계 각국의 제약사들이 개발중인 코로나19 백신들의 특징과 작용원리는 뭘까?
식약처는 7일 코로나19 백신의 특징과 작용원리에 대해 자세히 설명했다.
설명자료에 따르면 먼저 백신 플랫폼은 ▲바이러스벡터 백신 ▲RNA 백신 ▲재조합 백신 ▲불활화 백신 등이 있다.
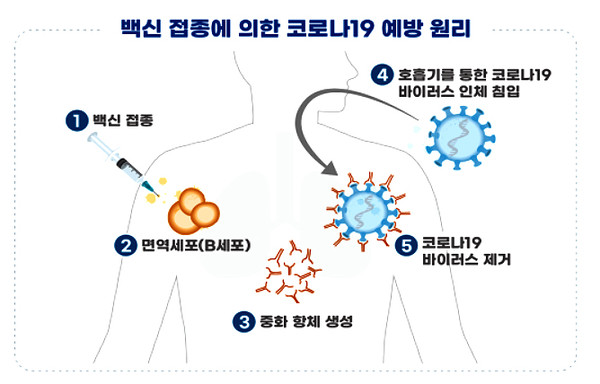
백신 접종에 의한 코로나19 예방원리는 ➊코로나19 백신 접종 ➋인체 내로 들어온 백신의 항원 성분들이 면역세포(B 세포) 자극 ➌자극된 B세포에서 바이러스를 제거할 수 있는 중화항체를 만들어서 몸속에 보관 ➍코로나19 바이러스가 호흡기를 통해 침입하는 경우 ➎ 몸속의 중화항체가 침입한 코로나19 바이러스를 제거되는 원리이다.
바이러스벡터 백신은 항원 유전자를 인체에 무해한 아데노바이러스 등 다른 바이러스 주형에 주입해 체내에서 항원 단백질을 생성함으로써 면역반응을 유도하는 백신으로, 대표적으로 아스트라제네카社 백신, 얀센(존슨앤드존슨) 백신 등이 있으며 한국에 도입 예정이다.
아스트라제네카 백신은 침팬지에게만 감염되는 아데노바이러스를 전달체로 사용했으며 RNA 백신에 비해 상대적으로 열에 안정적인 특징이 있으나, 살아있는 아데노바이러스를 사용하므로 생백신(4℃)에 준하는 콜드체인이 필요하며, 현재까지 허가된 백신으로는 얀센社의 에볼라 백신이 있다.
아스트라제네카 백신은 영국에서 2020년 12월 30일 긴급사용 승인했고, 유럽의약품청(EMA)도 지난해 10월부터 사전검토를 진행하고 있다고 알려져 있으며 국내에서는 지난 4일 허가 신청돼 현재 식약처가 품목허가 심사 중이다. 심사기간을 40일로 목표삼아 허가를 추진중이다.
얀센(존슨앤드존슨) 백신은 2020년 9월부터 3상 임상시험이 진행 중이며 현재까지 해외 허가승인 사례는 없다. 국내에서는 비임상·품질 자료에 대한 사전검토가 지난 12월22일 신청돼 검토 진행 중이다.
국내 개발로는 셀리드 백신이 임상 1/2상 진행 중에 있다.
RNA 백신은 항원 유전자를 RNA 형태로 주입해 체내에서 항원 단백질을 생성해 면역반응을 유도하는 백신으로, 대표적으로 화이자제약 백신, 모더나사 백신 등이 있으며 한국에 도입 예정이다.
제조 기간이 짧아 신속하게 단기간 내에 대량생산이 가능하나, RNA 분해효소(RNase)에 쉽게 주성분인 RNA가 분해되어 안정성이 좋지 않아 냉동((예) -20℃ 또는 –75±15℃)의 콜드체인 필요하며, 이 방식으로는 코로나19 백신이 처음으로 제품화 됐다. 여기서 RNA(Ribonucleic acid)는 유전자 정보를 매개, 유전자 발현 조절 등의 역할을 하는 세포의 핵 속에 있는 두 종류의 핵산 중 하나이다.
화이자 백신은 현재 긴급사용 승인된 국가는 영국(2020.12.02.), 미국(2020.12.11.), 캐나다(2020.12.09.) 등이 있고, 스위스(2020.12.19.) 및 유럽(EU)(2020.12.21.)에서는 조건부 허가됐다.
세계보건기구(WHO)도 긴급사용 승인(2020.12.31.)해 전 세계적으로 화이자 백신을 사용하고 있는 바, 보편적으로 참고 가능하다는 긍정적인 의미가 있다.
국내에서는 비임상·임상 자료에 대한 사전검토가 지난해 12월18일 신청돼 검토 진행 중이다.
모더나 백신은 현재 미국)에서 긴급사용승인이 됐고 유럽(EU)에서 6일 조건부 허가됐다.
국내에는 사전검토 및 품목허가 신청 전입니다. 국내 개발 백신으로는 RNA 백신과 유사한 형태의 DNA 백신을 제넥신과 진원생명과학에서 각각 개발 중이며 임상 1/2상 진행 중이다.
코로나19 백신으로는 노바백스 백신이 있으며 2020년 9월부터 3상 임상시험이 진행 중이며 현재까지 해외 허가승인 사례는 없으며 국내 개발로는 SK바이오사이언스 백신이 임상 1/2상 진행 중에 있다.
불활화 백신은 바이러스를 사멸시켜 항원으로 체내에 주입해 면역반응을 유도하는 전통적인 백신 플랫폼으로, 개발된 다수의 백신이 있다. 감염 바이러스 확보 시 신속 개발이 가능하고 제조방법이 단순하며, 중화항체 유도가 우수한 특징이 있으나, 코로나19 바이러스의 경우에는 BL3급의 생산시설이 필요하다. 불활화 백신으로는 A형 간염백신, 주사용 소아마비 백신, 일본뇌염 사백신 등이 있다.
코로나19 백신으로는 중국 시노팜 백신이 있으며, 중국에서 2020년 7월 22일에 허가됐다.
이 밖에도 WHO(COVID-19 후보 백신 업데이트)에 따르면 캔시노(바이러스벡터 백신), 러시아 가말레야 연구소(바이러스벡터 백신) 등에서 다양한 종류의 코로나19 백신이 개발 중에 있다.
코로나19 백신개발 플랫폼 종류
➊ (바이러스벡터 백신) 코로나19 바이러스의 표면항원 유전자를 다른 바이러스(아데노바이러스 등) 주형에 넣어 주입해 체내에서 표면항원 단백질을 생성함으로써 면역반응 유도예 : 아스트라제네카社(영국), 얀센社(미국)
➋ (불활화 백신) 사멸시킨 코로나19 바이러스를 체내 주입해 면역반응 유도예 : 시노팜社(중국)
➌ (DNA 백신) 코로나19 바이러스의 표면항원 유전자(DNA)를 주입해 체내에서 표면항원 단백질을 생성해 면역반응 유도예 : 이노비오社(미국)
➍ (RNA 백신) 코로나19 바이러스의 표면항원 유전자를 RNA 형태로 주입해 체내에서 표면항원 단백질을 생성해 면역반응 유도예 : 화이자社(미국), 모더나社(미국)
➎ (재조합 백신) 유전자재조합 기술을 이용해 만든 코로나19 바이러스의 표면항원 단백질을 직접 주입하여 면역반응 유도예 : 노바백스社(미국)
➏ (바이러스 유사입자 백신) 코로나19 바이러스 표면항원 단백질을 바이러스와 유사한 입자 모양으로 만들어 주입하여 면역반응 유도예 : 인도 혈청연구소



